Обмен углеводов играет важную роль в жизнедеятельности организма. Катаболизм углеводов, с одной стороны, сопровождается освобождением энергии, которая может накапливаться в макро-эргических связях АТФ и использоваться в дальнейшем для синтеза необходимых молекулярных компонентов клетки и совершения различных видов работы, с другой стороны, образующиеся метаболиты служат исходными веществами для образования биологически важных соединений, таких как аминокислоты, липиды, нуклеотиды.
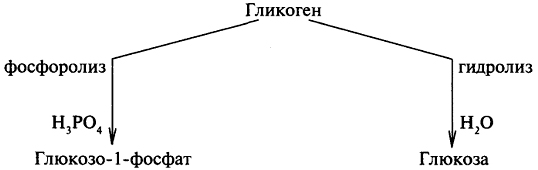
Гликогенолиз. Запасным полисахаридом в тканях человека является гликоген. Процесс распада гликогена называется гликогенолизом. Этот процесс может осуществляться либо путем гидролиза, либо фосфоролиза.
83
Фосфоролиз является основным путем распада гликогена, его катализирует фермент гликогенфосфорилаза, относящийся к классу трансфераз. Гликогенфосфорилаза отщепляет остатки глюкозы с нередуцирующего конца гликогена и переносит их на молекулу фосфорной кислоты с образованием глюкозо-1-фосфата:

Глюкозо-1-фосфат быстро изомеризуется, превращаясь в глюкозо-6-фосфат, который в печени гидролизуется фосфатазами до глюкозы и фосфорной кислоты:

Процесс фосфоролиза гликогена тонко регулируется. Регуляция активности гликогенфосфорилазы носит каскадный характер, в котором можно выделить несколько видов регуляции ферментативной активности:
84
- 1) гормональная (глюкагон в печени, адреналин в мышцах);
- 2) аллостерическая;
- 3) протеинкиназные реакции (в данном случае - фосфорилирование бокового радикала серина в гликогенфосфорилазе).
Активность мышечной фосфорилазы увеличивается при определенной концентрации АМФ и ацетилхолина, а также в присутствии катионов кальция и натрия.
Снижение скорости фосфоролиза происходит при уменьшении запасов гликогена и фосфорной кислоты, а также при увеличении концентрации глюкозо-6-фосфата. Механизмы, снижающие скорость фосфоролиза гликогена, предохраняют организм от больших трат углеводных запасов (гликогена), которые могли бы привести к недостатку глюкозы, необходимой для работы головного мозга и сердечной мышцы.
Гидролиз гликогена катализируется ферментами амилазами, которые относятся к классу гидролаз. В результате гидролиза гликоген расщепляется до свободной глюкозы:

Гидролитический распад гликогена происходит обычно в печени. Глюкоза, полученная при фосфоролизе и гидролизе гликогена, поступает в различные ткани и органы организма, где подвергается дальнейшему распаду.
Распад глюкозы возможен двумя путями. Один из них заключается в распаде шестиуглеродной молекулы глюкозы на две трехуглеродные молекулы. Этот путь называется дихотомическим
85
распадом глюкозы. При реализации второго пути происходит потеря молекулой глюкозы одного атома углерода, что приводит к образованию пентозы; этот путь носит название апотомическо-го распада.
Дихотомический распад глюкозы может происходить как в анаэробных (без присутствия кислорода), так и в аэробных (в присутствии кислорода) условиях. При распаде глюкозы в анаэробных условиях в результате процесса молочнокислого брожения образуется молочная кислота. Иначе этот процесс называется гликолизом (от греч. glicos - сладкий, lysis - растворение).
Отдельные реакции гликолиза катализируют 11 ферментов, образующих цепь, в которой продукт реакции, ускоряемой предшествующим ферментом, является субстратом для последующего. Гликолиз условно можно разбить на два этапа. В первом этапе происходит затрата энергии, второй этап, наоборот, характеризуется накоплением энергии в виде молекул АТФ (схема 1).
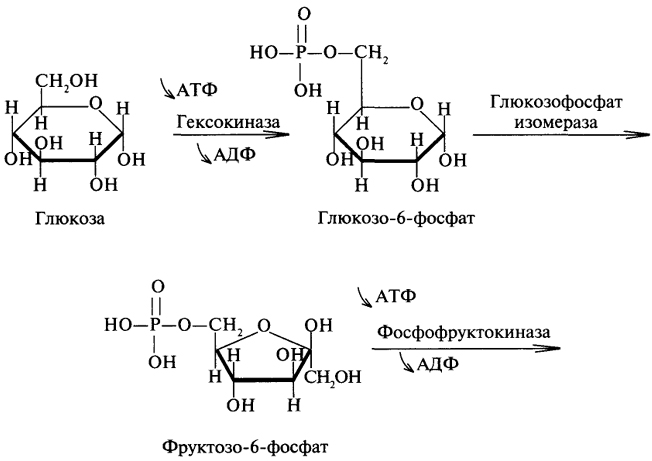
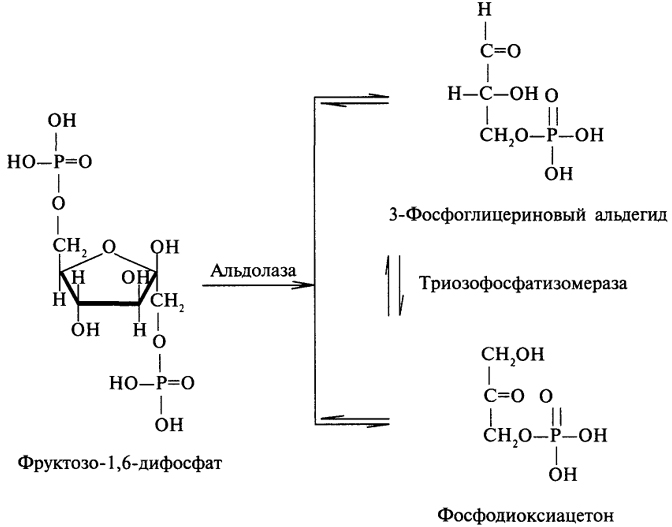
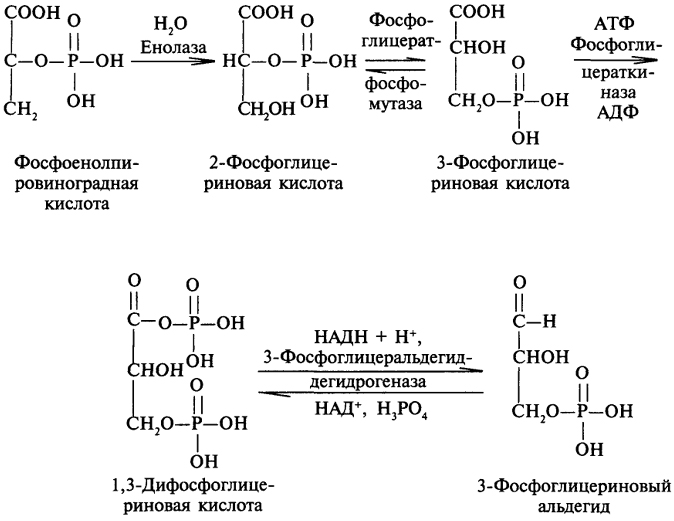
Первой реакцией гликолиза является фосфорилирование глюкозы с образованием глюкозо-6-фосфата. Глюкозо-6-фосфат далее изомеризуется во фруктозо-6-фосфат, который фосфорилируется до фруктозе-1,6-дифосфата. Следующей реакцией является лиазное расщепление фруктозо-1,6-дифосфата до двух триоз-3-фосфоглицеринового альдегида и фосфодиоксиацетона. Образованием этих триоз заканчивается первый этап гликолиза:
86
Во второй этап гликолиза вступают 2 молекулы 2-фосфоглицеринового альдегида, одна из которых образуется непосредственно при расщеплении фруктозо-1,6-дифосфата, а другая при изомеризации фосфодиоксиацетона.
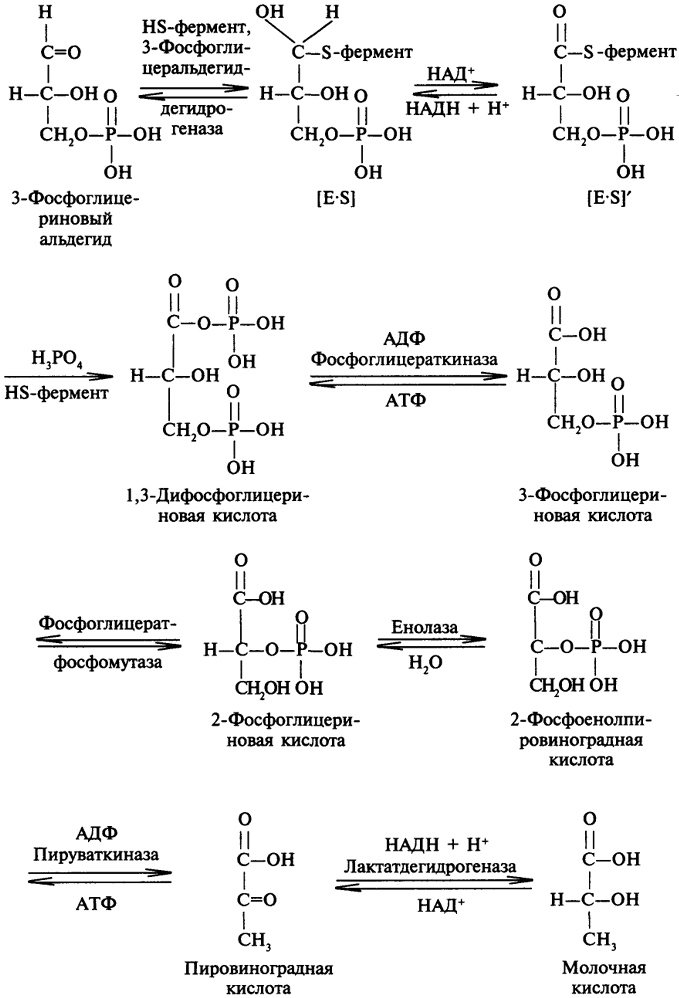
Второй этап гликолиза открывается реакцией окисления 3-фосфоглицеринового альдегида, катализируемой специфической дегидрогеназой, содержащей в активном центре свободную сульфгидрильную (HS-) группу и кофермент НАД. В результате образуется 1,3-дифосфоглицериновая кислота. Далее происходит перенос фосфатной группы на молекулу АДФ; таким образом происходит запасание энергии в макроэргических связях молекулы АТФ. Поскольку в гликолизе образуются 2 молекулы 1,3-дифосфоглицериновой кислоты, то и возникают 2 молекулы АТФ. Изомеризация предыдущего метаболита в 2-фосфоглицериновую кислоту необходима для протекания реакции дегидратации, ускоряемой соответствующей лиазой, с образованием макроэргического соединения - фосфоенолпировиноградной кислоты, которая далее отдает фосфатную группу на молекулу АДФ. В результате образуется по 2 молекулы АТФ и пировиноградной кислоты (ПВК). Заключительной реакцией этого метаболического пути является
87
молочная кислота, которая образуется при восстановлении пировиноградной кислоты:
88

Схема 1. Гликолиз
89
Бо́льшая часть молочной кислоты, образующейся в мышце, вымывается в кровяное русло. Изменению рН крови препятствует бикарбонатная буферная система: у спортсменов буферная емкость крови повышена по сравнению с нетренированными людьми, поэтому они могут переносить более высокое содержание молочной кислоты. Далее молочная кислота транспортируется к печени и почкам, где она почти полностью перерабатывается в глюкозу и гликоген. Незначительная часть молочной кислоты вновь превращается в пировиноградную кислоту, которая в аэробных условиях окисляется до конечных продуктов обмена.
Аэробный обмен ПВК. В аэробных условиях пировиноградная кислота окисляется; этот процесс называется окислительным декарбоксилированием пировиноградной кислоты. Катализирует этот процесс мультиэнзимный комплекс, который называется пируватдегидрогеназным комплексом. В состав этого комплекса входят три фермента и пять коферментов.
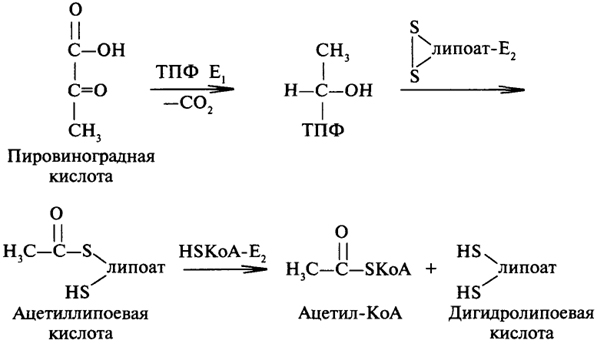
Первый этап аэробного превращения ПВК заключается в ее декарбоксилировании, катализируемом пируватдекарбоксилазой (E1), коферментом которой является тиаминпирофосфат. В результате образуется оксиэтильный радикал, ковалентно связанный с коферментом.
Фермент, ускоряющий второй этап окислительного декарбоксилирования ПВК, - липоат-ацетилтрансфераза содержит в своем составе два кофермента: липоевую кислоту и коэнзим A (KoASH). Происходит окисление оксиэтильного радикала в ацетильный, который сначала акцептируется липоевой кислотой, а затем переносится на KoASH. Результатом второго этапа является образование ацетил-КоА и дегидролипоевой кислоты:
90
Заключительную стадию окислительного декарбоксилирования ПВК катализирует дигидролипоилдегидрогеназа, коферментом которой является ФАД. Кофермент отщепляет два атома водорода от дигидролипоевой кислоты, тем самым воссоздавая первоначальную структуру данного кофермента:
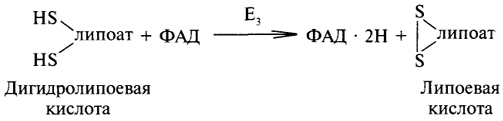
Конечным акцептором атомов водорода является НАД:
ФАД · 2Н + НАД+ → ФАД + НАДН + Н+
Суммарная схема процесса может быть представлена в виде:

Ацетил-КоА представляет собой соединение с макроэргической связью, иначе его можно назвать активной формой уксусной кислоты. Освобождение коэнзима А от ацетильного радикала происходит при включении его в амфиболический цикл, который называется циклом ди- и трикарбоновых кислот.
Цикл ди- и трикарбоновых кислот. Этот амфиболический цикл называют циклом Кребса в честь Г. Кребса (лауреата Нобелевской премии 1953 г.), определившего последовательность реакций в этом цикле.
В результате функционирования цикла Кребса происходит полный аэробный распад ацетильного радикала до углекислого газа и воды (схема 2). Цикл Кребса можно рассматривать как путь углеводного обмена, однако его роль в метаболизме гораздо шире. Во-первых, он выступает в роли центрального метаболического пути углерода, входящего в состав всех основных классов биологических молекул, во-вторых, совместно с процессом окислительного фосфорилирования обеспечивает основной источник метаболической энергии в форме АТФ.
Ферменты цикла ди- и трикарбоновых кислот, ускоряющие единый многоступенчатый процесс, локализованы во внутренней мембране митохондрий.
91

Схема 2. Цикл Кребса
Рассмотрим конкретные реакции цикла Кребса.
Превращения ацетил-КоА начинаются с реакции конденсации его со щавелевоуксусной кислотой, в результате которой образуется лимонная кислота. Эта реакция не требует расхода АТФ, так как необходимая для этого процесса энергия обеспечивается гидролизом тиоэфирной связи с ацетил-КоА, которая, как мы уже отмечали, является макроэргической:

92
Далее происходит изомеризация лимонной кислоты в изолимонную. Фермент данного превращения - аконитаза - сначала дегидратирует лимонную кислоту с образованием цис-аконитовой кислоты, затем присоединяет воду к двойной связи полученного метаболита, образуя изолимонную кислоту:

Изолимонная кислота подвергается окислению при участии специфической дегидрогеназы, коферментом которой является НАД. Одновременно с окислением происходит декарбоксилирование изолимонной кислоты. В результате этих превращений образуется α-кетоглутаровая кислота.

Следующей стадией является окислительное декарбоксилирование α-кетоглутаровой кислоты. Катализируется этот процесс α-кетоглутаратдегидрогеназным комплексом, который аналогичен по структуре и механизму действия пируватдегидрогеназному комплексу. В результате этого процесса образуется сукцинил-КоА:

93
Сукцинил-КоА далее гидролизуется до свободной янтарной кислоты, а выделяющаяся при этом энергия сохраняется путем образования гуанозинтрифосфата (ГТФ). Эта стадия - единственная во всем цикле, в ходе которой прямо выделяется энергия метаболизма:
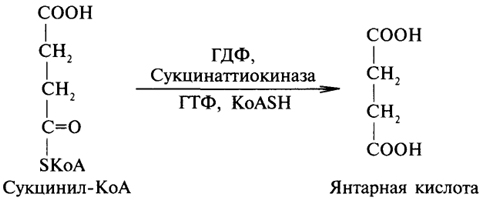
Дегидрирование янтарной кислоты ускоряет сукцинатдегидрогеназа, коферментом которой является ФАД. Фумаровая кислота, образовавшаяся при дегидрировании янтарной кислоты, гидратируется с образованием яблочной кислоты; заключительным процессом цикла Кребса является дегидрирование яблочной кислоты, катализируемое малатдегидрогеназой; результатом этой стадии является метаболит, с которого и начался цикл ди- и трикарбоновых кислот - щавелевоуксусная кислота:

Апотомический распад глюкозы иначе называется пентозофосфатным циклом. В результате протекания этого пути из 6 молекул глюкозо-6-фосфата распадается одна. Апотомический распад можно разделить на две фазы: окислительную и анаэробную. Рассмотрим отдельные реакции этого метаболического пути.
Окислительная фаза апотомического распада глюкозы. Как и в гликолизе первой стадией является фосфорилирование глюкозы с образованием глюкозо-6-фосфата. Далее глюкозо-6-фосфат дегидрируется с участием глюкозо-6-фосфатдегидрогеназы, коферментом которой служит НАДФ. Образующийся 6-фосфоглюконолактон спонтанно или с участием лактоназы гидролизуется с образованием 6-фосфоглюконовой кислоты. Заключительным
94
процессом окислительной ветви пентозофосфатного цикла является окисление 6-фосфоглюконовой кислоты соответствующей дегидрогеназой. Одновременно с процессом дегидрирования происходит декарбоксилирование 6-фосфоглюконовой кислоты. С потерей одного углеродного атома глюкоза превращается в пентозу:

Анаэробная фаза анатомического распада глюкозы. Рибулозо-5-фосфат, образовавшийся в окислительной фазе, может обратимо изомеризоваться в другие пентозофосфаты: ксилулозо-5-фосфат и рибозо-5-фосфат. Катализируют эти реакции два разных фермента, относящиеся к классу изомераз: пентозофосфат изомераза и пентозофосфат эпимераза. Образование из рибулозо-5-фосфата двух других пентозофосфатов необходимо для осуществления последующих реакций пентозофосфатного цикла, причем требуется две молекулы ксилулозо-5-фосфата и одна молекула рибозо-5-фосфата.
95

Далее идут реакции с участием ферментов трансфераз, переносящих молекулярные остатки - трансальдолазы и транскетолазы. Укажем, какие молекулярные остатки переносят эти ферменты.
Транскетолаза переносит двухуглеродный фрагмент от 2-кетосахара на первый углеродный атом альдозы. Трансальдолаза переносит трехуглеродный фрагмент от 2-кетосахара на первый атом углерода альдозы. В качестве 2-кетосахара используется ксилулозо-5-фосфат и метаболиты, полученные при ее участии.
Рассмотрим некоторые реакции, катализируемые транскетолазой и трансальдолазой.
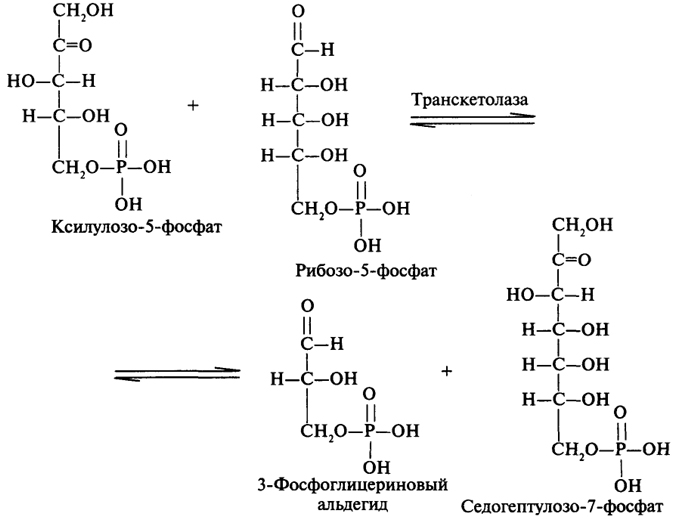
96

97
Фруктозо-6-фосфат и 3-фосфоглицериновый альдегид включаются в гликолиз. Оба пути обмена углеводов тесно связаны (схема 3).

Схема 3. Взаимосвязь гликолиза и пентозофосфатного цикла
Распад глюкозы по апотомическому пути в большей степени наблюдается в жировой ткани, печени, ткани молочной железы, надпочечниках, половых железах, костном мозге, лимфоидной ткани. Низкая активность отмечается в мышечной ткани (сердечной и скелетной мышце).
Биологическое назначение пентозофосфатного цикла связано с образованием восстановленной формы НАДФ и рибозо-5-фос-фата, которые используются в процессах биосинтеза разнообразных биологических молекул. Кроме того, апотомический распад глюкозы выполняет энергетическую функцию, так как некоторые
98
из его продуктов, прежде всего 3-фосфоглицериновый альдегид, подключаются к гликолизу.
В тканях и органах человека происходит синтез сложных углеводов. Строительным блоком (мономерным звеном) для синтеза служит глюкоза. Большая часть глюкозы поступает в организм человека с пищей, однако при длительном голодании может включаться механизм синтеза глюкозы из неуглеводных источников.
Глюконеогенез - процесс новообразования глюкозы из неуглеводных источников. В качестве субстратов глюконеогенеза могут служить аминокислоты, превращающиеся в пировиноградную и в щавелевоуксусную кислоты; такие аминокислоты называются гликогенными. К гликогенным относятся все протеиногенные аминокислоты, кроме лейцина. Также к неуглеводным источникам глюконеогенеза относятся глицерин, кислоты цикла Кребса, молочная кислота. Преобразование всех указанных веществ (кроме глицерина) в глюкозу проходит через стадию пировиноградной и щавелевоуксусной кислот.
Большая часть реакций на пути от пирувата до глюкозы катализируется ферментами гликолиза путем обращения соответствующих реакций. Однако нормальный путь гликолиза ("сверх вниз") включает 4 необратимых этапа, которые не могут быть использованы в глюконеогенезе, идущем "снизу вверх". Это реакции, катализируемые гексокиназой, фосфофруктокиназой, фосфоглицераткиназой и пируваткиназой; в глюконеогенезе эти этапы осуществляются обходными путями.
Превращение ПВК в фосфоенолпировиноградную кислоту происходит через стадию образования щавелевоуксусной кислоты:

Далее фосфоенолпировиноградная кислота превращается в фосфотриозы, которые дают фруктозо-1,6-дифосфат:
99
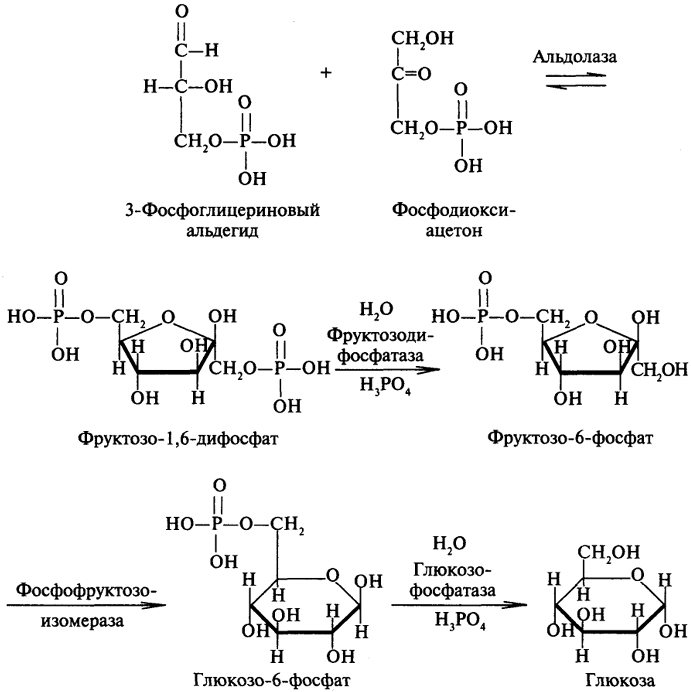
Для образования фруктозе-1,6-дифосфата требуется две молекулы 3-фосфоглицеринового альдегида, одна из которых превратится в фосфодиоксиацетон при участии фермента триозофосфатизомеразы:

Далее из этих двух фосфотриоз образуется фруктозо-1,6-дифосфат. На последних стадиях глюконеогенеза "работают" ферменты фосфатазы, которые не представлены в гликолизе. Это еще один факт, подтверждающий самостоятельность глюконеогенеза:
100
Глюконеогенез - регулируемый процесс, на скорость протекания которого оказывают влияние гормоны. Инсулин тормозит образование углеводов из аминокислот, кортикостероиды, наоборот, стимулируют глюконеогенез.
Столь подробное рассмотрение процесса глюконеогенеза связано с тем, что этот метаболический путь использует молочную кислоту, накапливающуюся в мышцах во время интенсивной мышечной работы. Следовательно, глюконеогенез, протекающий в печени, можно рассматривать как приспособление для разгрузки организма от молочной кислоты, образующейся в мышцах в анаэробных условиях.
Биосинтез гликогена. Иначе биосинтез гликогена называется гликогеногенезом. Он осуществляется практически во всех тканях,
101
но особенно активно протекает в скелетных мышцах и в печени. Биосинтез гликогена может идти двумя путями. Один из них заключается в переносе олигосахаридных фрагментов с одного полисахарида на существующий фрагмент гликогена, другой - в переносе остатков глюкозы. Источником остатков глюкозы служит уридиндифосфатглюкоза (УДФ-глюкоза), которая образуется из глюкозо-1-фосфата и УТФ при участии фермента глюкозо-1-фосфатуридилтрансферазы:
Глюкозо-1 -фосфат + УТФ → УДФ-глюкоза + Н4Р2О7
Синтез гликогена осуществляет фермент гликогенсинтетаза. Фермент снимает остаток глюкозы с УДФ-глюкозы и переносит его на нередуцирующий конец растущей цепи гликогена:

102
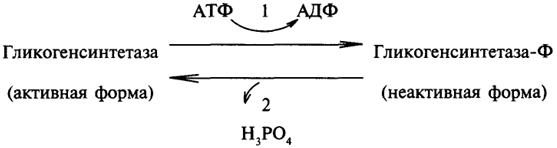
Активность гликогенсинтетазы регулируется за счет реакций фосфорилирования - дефосфорилирования. Активной формой гликогенсинтетазы является ее дефосфорилированная форма. Эти процессы катализируют два фермента: киназа гликогенсинтетазы (1) и фосфатаза гликогенсинтетазы (2).
Гликогенсинтетаза ведет синтез цепи амилозного типа. Разветвленная структура образуется путем переноса полиглюкозидной цепи у α-1,4-глюкана из положения 4 в положение 6. Этот механизм реализуется с помощью фермента, который называется α-1,4-глюканветвящий фермент. Трансгликозилирование, катализируемое этим ферментом, можно схематично представить следующим образом (рис. 13).
Интеграция разных путей обмена углеводов в организме. Интенсивность катаболических и анаболических путей обмена углеводов в разных тканях организма неодинакова и определяется прежде всего особенностями обмена каждой ткани и органа. Если рассматривать организм в целом, то можно выявить некоторую специализацию путей превращения углеводов в отдельных тканях. Такая специализация, несомненно, оправдана, так как отвечает функциональной направленности ткани или органа. Поскольку функционирование отдельных органов обеспечивает жизнедеятельность всего организма, существенным моментом в обмене веществ в целом и в обмене углеводов в частности является интеграция катаболических и анаболических процессов.
Приведем пример. При активной мышечной работе затрачиваются большие количества энергии, которая первоначально извлекается в ходе распада гликогена до молочной кислоты.

Рис. 13. Схема действия α-1,4-глюканветвящего фермента.
103
Молочная кислота, как говорилось выше, вымывается в кровь, которая доставляет ее в печень, где происходит синтез глюкозы в ходе глюконеогенеза. Глюкоза из печени переносится кровью в скелетные мышцы, где либо расходуется на образование энергии, либо запасается в виде гликогена. Этот межорганный цикл в обмене углеводов получил название цикла Кори:
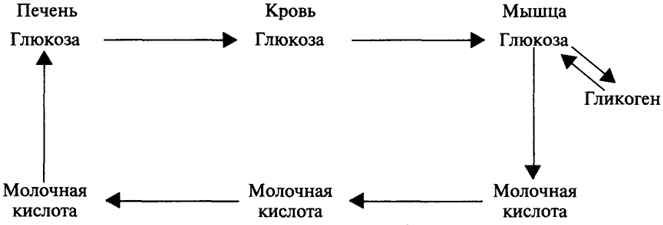
Схема 4. Цикл Кори
Функция мышечного гликогена заключается в том, что он является легкодоступным источником глюкозы для самой мышцы. Гликоген печени используется главным образом для поддержания физических концентраций глюкозы в крови в основном в промежутках между приемами пищи. Через 12 - 18 ч после приема пищи запас гликогена в печени почти полностью истощается. Содержание мышечного гликогена заметно снижается только после продолжительной и напряженной физической работы. Повышенное содержание гликогена в мышцах может наблюдаться при диете с высоким содержанием углеводов, если перед этим запасы гликогена были снижены в результате высокой мышечной нагрузки.
104
