Электрокоагуляция - один из приемов электрохимической очистки воды. Она обеспечивает нарушение седиментационной и агрегативной устойчивости дисперсных систем, что приводит к образованию крупных легко удаляемых хлопьев загрязнений, не изменяя при этом природу сложных физико-химических процессов коагуляции.
В инженерной практике чаще всего электрокоагуляторы используют как аппараты, позволяющие генерировать и дозировать коагулянт за счет электрохимического растворения металлических электродов. Поэтому наибольший практический интерес представляют основы расчета электрохимических генераторов коагулянта.
Исходными данными для расчета электрогенератора коагулянта (ЭГК), как правило, являются производительность установки (Q, м3/ч), состав исходной воды (тип и концентрации примесей, подлежащих удалению), состав воды после обработки или степень очистки воды по основным загрязняющим веществам.
Порядок выполнения расчетов может быть представлен следующей последовательностью шагов:
- - выбор материала электродов;
- - оценка дозы генерируемого коагулянта;
- - выбор рабочей плотности тока;
- - расчет параметров электрохимического генератора коагулянта (оценка рабочего тока - Iраб, и рабочего напряжения - Uраб);
- - подбор источника тока;
- - расчет габаритов электролизной ванны;
- - расчет газовыделения;
- - расчет тепловыделения.
Выбор материала электродов равнозначен выбору типа коагулянта для обработки каждого конкретного потока воды.
Поскольку современное состояние теории коагуляции не позволяет расчетными методами однозначно обосновывать выбор типа коагулянта, рекомендуется проведение предварительных опытных проверок, например, методами пробной коагуляции. Возможно и использование практических результатов обработки аналогичных по природе систем, приводимых в литературе. Для типичных случаев можно воспользоваться рекомендациями, некоторые из которых приведены в таблице 18.10.1.
Таблица 18.10.1
Параметры работы электрокоагулятора при очистке некоторых категорий сточных вод
| Категория обрабатываемых вод |
Рекомендуемая
величина рН
обрабатываемой
воды |
Расход тока
Дт, Кл/л |
Плотность
тока,
А/м2 |
Расход
электроэнергии
Wэл, кВт-ч/м3 |
Напряжение,
В |
Расход металла
электродов,
(доза коагулянта) Дт1, г/м3 |
Материал
электродов |
Расстояние
между электродами
lэ, мм |
| Подготовка питьевой воды (обесцвечивание, обезжелезивание, умягчение) |
7-8 |
10-90 |
6- 12,5 |
0,4-2,5 |
10-12 |
3-20 |
Алюминий, графит, железо, ОРТА и др. |
10-15 |
169
В последние годы в практике использования электрокоагуляционных процессов стали обращать внимание на использование электродов сложного состава - сплавов различных металлов или композиций различных металлов. Применение сложных композиционных материалов при обработке водных потоков представляется весьма перспективным направлением, поскольку значительно расширяет круг свойств рабочих материалов (коагулянтов) по сравнению с возможностями чистых компонентов. Электрохимическое растворение сплавов характеризуется большими, нежели для чистых компонентов, выходами по току.
На рис. 18.10.1 и 18.10.2 представлены экспериментальные данные по изменению величины стационарного потенциала φстац, скорости электрохимического растворения Fe-Al сплавов υFe-Аl, гидравлической крупности образующихся агрегатов U и удельной поверхности коагуляционных хлопьев Sуд от состава бинарного сплава. Из приведенных на рисунках экспериментальных данных видно, что все полученные зависимости имеют нелинейный характер, сложным образом зависят от состава сплава.

Рис. 18.10.1. Выбор оптимального растворимого анодного материала.
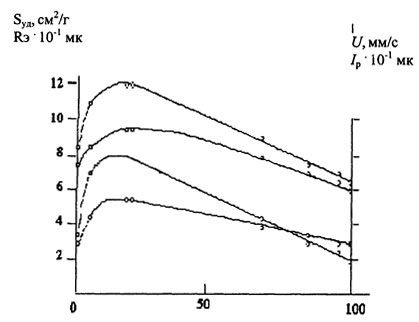
Рис. 18.10.2. Влияние состава Fe-Al сплавов на гидродинамические и адсорбционные характеристики электрогенерируемых коагулянтов.
Растворение железо-алюминиевых сплавов в области образования химического соединения Fe3Al (область максимумов на представленных зависимостях) сопровождается образованием коагулянта с более высокими гидродинамическими характеристиками, чем растворение алюминия, железа и их сплавов иного состава. А именно, гидравлическая крупность образующихся хлопьев коагулянтов или скорость их осаждения выше, чем эти показатели для коагулянтов, полученных при электрохимическом растворении алюминиевых и железных анодов, в 2,5-3,0 и 1,8-2,0 раза соответственно. Коагулянты, полученные
170
при растворении сплавов в области образования химического соединения Fe3Al, обладают более высокой удельной поверхностью Sуд по сравнению с коагулянтами другого состава, что свидетельствует об их более высокой адсорбционно-коагулирующей способности.
Доза коагулянта это минимально необходимая концентрация коагулянта в обрабатываемом потоке в г/м3 (мг/л), при которой происходит интенсивное хлопьеобразование гидроксидов металла, способных за счет физико-химического взаимодействия с примесями концентрировать и удалять их в отдельную фазу (пену или осадок).
Дозу коагулянта для электрокоагуляционных процессов иногда выражают также через единицы количества электричества: Кл/литр (кулон на литр, амперсекунда на литр) или А·час/м3 (амперчас на кубический метр). Перевод одних единиц в другие базируется на законе Фарадея, который связывает массу электрохимически растворенного металла и количество пошедшего на этот процесс электричества
М = Мме · I · t · η / n · F = E · I · t · η
(18.10.1)
где М - масса выделяемого коагулянта; Mме - грамм.-молекулярный вес металла (алюминия МАl = 27, железа МFе = 56), г/моль; F - число Фарадея, F = 96500 А·сек/моль = = 26,8 А·ч/моль; Е - электрохимический эквивалент растворяемого металла, г/А·ч, г/ А·сек.; I - сила тока A; t - время, час (или секунды); η - выход по току (обычно η = 0,8-0,9); п - валентность, выделяемых в раствор ионов металла. Для Fe+2 n = 2, для А1+3 n = 3.
При электрохимическом растворении сплавов в первом приближении можно принимать, что растворение каждого из основных компонентов сплава идет пропорционально процентному содержанию компонента в сплаве. Например, при растворении железоалюминиевого сплава с содержанием алюминия 20 % масса выделяемого металла будет составлять:
М = MFe + MAl = (0,8 · MFe · I · t · η / n · F) + (0,2 · МАl · I · t · η / n · F).
(18.10.2)
Определение дозы коагулянта может быть произведено по стандартным методикам СНиП. Однако при этом надо помнить, что расчетная доза относится к количеству соли (сульфат алюминия или хлорид железа), которую используют в качестве коагулянта. Для использования этих величин при расчете электрокоагуляционных процессов необходимо расчетное количество соли - коагулянта пересчитывать в расчетное количество металла, содержащегося в этой соли.
Например, расчетная доза коагулянта - сульфата алюминия - составляет 150 г/м3. Формула сульфата алюминия - Al2(SO4)3. Учитывая, что молекулярные веса элементов, входящих в молекулу сульфата алюминия составляют: А1 = 27; S = 32; О = 16, определим молекулярный вес сульфата алюминия и кислотного аниона SO4-2
MAl2(SO4)3 = 2 · 27 + 3 · (32 + 4 · 16) = 342
(18.10.3)
MSO4 = 96.
Составляя пропорцию
342 - 54
150 - МAl
найдем массу алюминия в 150 граммах сульфата алюминия:
MAl = 150 · 54 / 342 = 23,684 г.
Следовательно, расчет электрогенератора коагулянта надо вести на дозу 23,684 г/м3.
Однако наиболее правильный и точный результат определения дозы коагулянта может быть получен при проведении пробных коагуляций. Это особенно необходимо
171
делать при использовании электродов сложного состава, например из сплавов, поскольку эффективность работы коагулянта зависит и от соотношения компонентов сплава, переходящих в раствор при электрорастворении анодов.
При электрокоагуляции генерация коагулянта происходит за счет растворения металлических рабочих электродов. Электрохимическое растворение металлов включает в себя две основные группы процессов: анодное растворение за счет действия электрического тока и химическое растворение в результате взаимодействия материала электрода с окружающей средой (водным раствором).
Анодное растворение металла под действием электрического тока - это процесс окисления материала анода, приводящий к образованию ионов металла (Ме+n) на границе раздела двух фаз: твердой - электрод и жидкой - обрабатываемая среда.
Ме0 - n e = Ме+n
Сила тока - определяется величиной потенциала электрода, скоростью отвода продуктов реакции и скоростью взаимодействия продуктов реакции с элементами окружающей среды.
В определенных условиях при увеличении потенциала наступает резкое падение скорости анодного растворения металла. Это явление называется пассивацией металла. Пассивация связана с изменением состояния поверхности электрода. Типичная поляризационная кривая представлена на рис. 18.10.3. На этой кривой можно выделить область увеличения тока с ростом анодного потенциала (I) (активная область); область перехода от активного состояния к пассивному (II); область пассивации (III), в которой ток растворения металла мал и часто практически не зависит от потенциала, и, наконец, область анодного выделения кислорода (область разряда воды) (IV). Если раньше анодного выделения кислорода наступает вновь растворение металла (пунктирная кривая), то промежуточная область IIIа называется областью перепассивации или транспассивности. Механизмы растворения металла в активной зоне и в области перепассивации могут значительно отличаться.
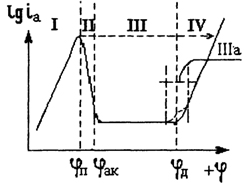
Рис. 18.10.3. Потенциостатическая поляризационная кривая.
Наиболее часто применяемые в практике электрокоагуляции электродные материалы А1 и Fe обладают существенным недостатком - высокой способностью к пассивации. Это осложняет эксплуатацию электрокоагуляционных установок, снижает эффективность и повышает энергоемкость процесса. Использование сплавов или композиционных анодов уменьшает склонность электродов к пассивации, однако, не исключает этого явления полностью.
В качестве примера на рис. 18.10.4 и 18.10.5 представлены реальные поляризационные кривые растворения алюминия и железа.
При выборе рабочих плотностей тока можно пользоваться и методом аналогий с подобными технологическими процессами, однако, метод непосредственных измерений гораздо более точен и надежен.
Расчет рабочего тока (Iраб) электрохимического генератора коагулянта производится исходя из часовой производительности установки (Qчас, м3/ч) и необходимой дозы коагулянта (Дк, г/м3).
172
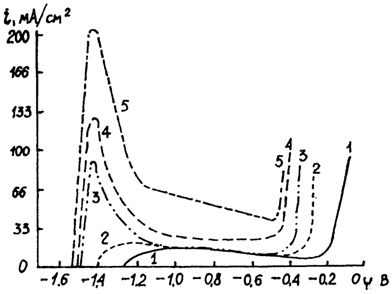
Рис. 18.10.4. Анодные поляризационные кривые растворения алюминия в растворах NaCl различной концентрации:
1-0,001 моль/л; 2-0,01 моль/л; 3-0,1 моль/л; 4-0,5 моль/л; 5-1,0 моль/л.
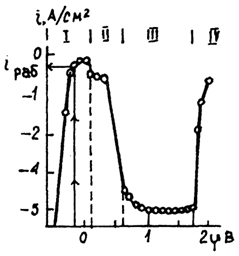
Рис. 18.10.5. Анодные поляризационные кривые растворения железа в 0,5 н H
2SO
4: I - зона активного растворения; II - переходная область; III - область пассивации; IV - область анодного выделения кислорода.
Масса коагулянта (Mк, г/ч), которую необходимо генерировать ежечасно для обеспечения необходимой производительности установки равна
Мк = Дк · Qчас.
(18.10.4)
Величина рабочего тока (Iраб) может быть определена по формуле
Iраб = Мк · n · F / (M.Me · t · η),
(18.10.5)
где М к - масса выделяемого коагулянта; MMе - грамм-молекулярный вес металла (алюминия МAl = 27, железа MFe = 56), г/моль; F - число Фарадея, F = 96500 А·ч/моль = 26,8 А·ч/моль; Iраб - сила тока, A; η - КПД выход по току (обычно η = 0,8-0,9); п - валентность, выделяемых в раствор ионов металла; t = 1 - расчетное время, часы.
Определенный таким образом рабочий ток позволяет в первом приближении оценить структуру электрогенератора коагулянта. Например, целесообразно разбиение его на отдельные секции, работающие параллельно друг другу, если Iраб превышает величину 2500-3000 А.
Рабочее напряжение электрогенератора коагулянта (Uраб) складывается из следующих основных составляющих: разность между равновесными электродными потенциалами анода (φа) и катода (φк) с учетом перенапряжения протекающих анодных (ήа) и катодных (ήк) реакций, падения напряжения на преодоление электрического сопротивления обрабатываемого раствора (Uраст), падения напряжения на материале электродов (Uа, Uк), падения напряжения на контактах (Uконт) и токоподводящих шинах (Uш).
Uраб = (φа - φк + ήа + ήк) + Uраст + Ua + Uк + Uконт + Uш.
(18.10.6)
Равновесные электродные потенциалы определяются процессами, протекающими на аноде и катоде электрохимической ячейки. Наиболее точно они могут быть рассчитаны
173
по изменению изобарного потенциала (потенциала Гиббса - ΔG) протекающих на электродах реакций.
Например, при электролизе кислых водных растворов на катоде происходит разряд ионов водорода: 2Н+ + 2е- Н2, а на аноде молекулы воды: Н2О - 2е- 2Н+ + ½O2.
Используя справочные величины значений свободных энергий (ΔG0) для исходных и конечных продуктов реакции (для Н2 ,О2 и Н+ ΔG0 = 0, для Н2О ΔG0 = - 56,69 ккал/моль, для ОН- ΔG0 = -37,585 ккал/моль) /10,11,12/, имеем:
- катодный процесс ΔGк0 = ΔGH20 - ΔGH+0 = 0 ккал/моль;
φк0 =
= 0 B;
- анодный процесс ΔGa0 = ½ΔGO20 + 2ΔGH+0 - ΔGH2O0 = -56,69 ккал/моль;
φa0 =
= 1,23 B;
При переходе от стандартных условий протекания процесса (P = 0,1МПа Т= 25 °С, активность электролита а = 1) к рабочим температурам и концентрациям можно использовать уравнение Нернста.
φ = φ0 +2,3 · (RT/nF) · lgaI,
(18.10.7)
Для рассматриваемого примера равновесные электродные потенциалы имеют значения:
- катодный φк = φк0 + 2,3
lg aH+ = 0 - 2,3
рН = -0,058
рН В;
- анодный φa = φa0 + 2,3
lg aH+ = 1,23 - 2,3
рН = 1,23 -0,058
рН В;
Стандартные потенциалы многих электродных реакций могут быть найдены в справочниках, например, /12/.
Падение напряжения в растворе (UpaCT ) для бездиафрагменных электролизных аппаратов вносит наиболее существенный вклад в суммарное падение напряжения и может быть рассчитано по выражению:
Uраст = i / æ · lэ · σг
(18.10.8)
где i - рабочая плотность тока, А/м2; æ - электропроводность обрабатываемого раствора, Ом/м (размерность может быть выражена в сименсах, См·м-1; lэ - расстояние между электродами, м; σг - коэффициент газосодержания межэлектродного пространства, который учитывает изменение электропроводности за счет газа, выделяющегося в процессе электролиза. Коэффициент может быть рассчитан по эмпирической формуле
σг = (1-Г)3/2,
(18.10.9)
где Г - газосодержание, величина которого может быть оценена выражением:
Г = Эоб · iк · t / qуд = (Vг / nк · F) · iк · t / qуд,
(18.10.10)
в котором Эоб - объемный электрохимический эквивалент выделяющегося газа при рабочей температуре и давлении, м3/моль (для электрогенераторов коагулянта таким газом является водород, объемный электрохимический эквивалент которого в стандартных условиях равен 0,0112 м3/моль); Vг - объем, который занимает 1 моль газа в рабочих условиях, м3; nк - число электронов, участвующих в катодном процессе газовыделения, F - число Фарадея, F = 96500 А·сек/моль = 26,8 А-ч/моль; iк - катодная рабочая плотность тока, А/м2; t -расчетное время, час; qул - удельный часовой расход обрабатываемой воды через единичную ячейку, образованную одной парой электродов генератора коагулянта, м3/час.
174
Среднее газосодержание межэлектродного пространства составляет Г = 0,01-0,04, и незначительно влияет на электропроводность, однако при малых расстояниях между электродами (менее 5 мм) влияние газосодержания может резко возрастать и его учет становится обязательным.
Для определения падения напряжения в растворе можно использовать графические методы. Номограмма на рис. 18.10.6 позволяет получать необходимые результаты с достаточной инженерной точностью.
Потери напряжения на электродах и токоподводящих шинах (Uа, Uк, Uш) рассчитывается по закону Ома:
U = Ipa6 · ρпр · lпр / Sпp,
(18.10.11)
где Iраб - рабочий ток установки, А; ρпр - удельное сопротивление проводника (электрода или шины), Ом·мм2·м-1; lпр - длина проводника, м; Sпр - сечение проводника, мм2.
Характеристики некоторых наиболее распространенных материалов приведены в табл. 18.10.2.
Падение напряжения на контактах электрической цепи (Uконт), как правило, тоже невелико и может быть посчитано по формуле:
Uконт = Iраб · ρконт,
(18.10.12)
где Iраб - рабочий ток, А; ρконт - удельное сопротивление контакта, Ом·мм2.
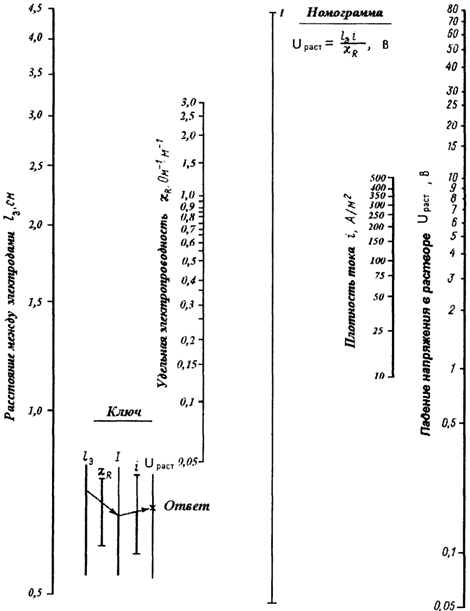
Рис. 18.10.6. Номограмма для определения падения напряжения в растворе.
175
Таблица 18.10.2.
Удельное сопротивление и допустимые плотности тока
для основных токопроводящих материалов
| Материал |
Удельное сопротивление, Ом·мм2·м-1 |
Допустимая плотность рабочего тока, А·мм-2 |
| Алюминий |
0,026 - 0,029 |
2,0 |
| Медь |
0,017 - 0,018 |
3,0 |
| Сталь (железо) |
0,103 - 0,140 |
1,5 |
| Латунь |
0,031 - 0,079 |
|
Величина ρконт зависит от удельного давления в контакте, состояния соприкасающихся поверхностей, температуры и ряда других факторов. Например, при удельном давлении 50 кг/см2 и температуре 25°С ρконт для некоторых пар материалов принимает следующие значения: "медь-медь" - 0,05, "алюминий-алюминий" - 0,5, "медь-титан" -0,1, "медь-графит" - 1,25.
Величина общего рабочего напряжения позволяет прежде всего выбрать и обосновать схему соединения электродов в электрохимической установке.
На рис. 18.10.7 представлены основные схемы подключения электродов к источнику питания.
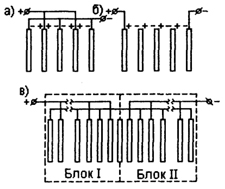
Рис. 18.10.7. Схемы подключения электродов:
а - монополярная,
б - биполярная,
в - комбинированная.
Наиболее часто на практике используется монополярное соединение.
Биполярное соединение (расчетное рабочее напряжение находится в пределах 2-5 В), снижая рабочие токи, требует повышения рабочих напряжений на источнике питания установки. При этом необходимо учитывать, что максимальное допустимое напряжение на электролитической ячейке согласно /13/ не должно превышать 36 В.
Комбинированные схемы позволяют оптимизировать нагрузки на источнике питания и повысить КПД используемых выпрямительных агрегатов.
Габаритные размеры ЭГК могут быть рассчитаны на базе результатов выбора материала рабочих электродов, подбора необходимой дозы коагулянта - Дк, г/м3, результатов выбора рабочей плотности тока (раздел 18.10.3) - iраб, А/м , расчетного рабочего тока установки Iраб, А., и заданной производительности установки, Q, м3/час.
Исходя из величины рабочего тока (Iраб) и рабочей плотности тока (/раб) находим величину поверхности рабочих электродов (анодов- Sа), обеспечивающих генерацию необходимой дозы коагулянта в установке:
Sa = Iраб / iраб.
(18.10.13)
Одним из основных условий оптимальной работы электролизера является то, что проходное сечение межэлектродного зазора (Sпр) должно при заданной производительности Q обеспечивать турбулентный режим течения жидкости.
Для каналов прямоугольного сечения критерий турбулентности потока по Рейнольдсу определяется минимальным значением скорости потока (vmin):
Reкр = · 4Rг ≥ 2800,
(18.10.14)
откуда
176
vmin ≥ ≥ 2800 · v / 4Rг,
(18.10.15)
где vmin - минимальная скорость потока жидкости в межэлектродном зазоре генератора коагулянта, при которой режим течения жидкости остается турбулентным (рис. 18.10.9); v - кинематический коэффициент вязкости обрабатываемого потока; Rг - гидравлический радиус прямоугольной ячейки.
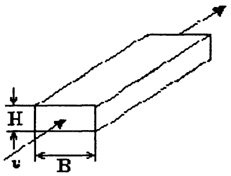
Рис. 18.10.9. Элементарная проходная ячейка электрогенератора коагулянта.
При проведении расчетов для водных потоков с умеренными концентрациями примесей величина кинематического коэффициента вязкости может быть принята равной кинематическому коэффициенту вязкости для воды. Высокие концентрации примесей, особенно таких, как СПАВ или нефтепродукты, может потребовать существенной корректировки этой характеристики.
Значения кинематического (v) и динамического (μ) коэффициентов вязкости воды приведены в таблице 18.10.3.
Таблица 18.10.3.
| t, град. |
V, см с-1 |
μ, г·см-1·с-1 |
t, град. |
V, см с-1 |
μ, г·см-1·с-1 |
t, град. |
V, см с-1 |
μ, г·см-1·с-1 |
| 2 |
0,01673 |
0,01673 |
10 |
0,01308 |
0,01308 |
18 |
0,01056 |
0,01057 |
| 4 |
0,01567 |
0,01567 |
12 |
0,01236 |
0,01237 |
20 |
0,01005 |
0,01007 |
| 6 |
0,01473 |
0,01473 |
14 |
0,01171 |
0,01172 |
22 |
0,00958 |
0,00960 |
| 8 |
0,01386 |
0,01386 |
16 |
0,01111 |
0,01112 |
24 |
0,00914 |
0,00917 |
Задаемся шириной электрода (В) и расстоянием между электродами (H), которые определяют сечение элементарной проходной ячейки и оцениваем критические гидродинамические параметры потока в элементарной ячейке в процессе работы генератора коагулянта.
Величина гидравлического радиуса элементарной ячейки (Rг) может быть определена по выражению:
Rг = B · H / 2(B + H),
(18.10.16)
Устойчивость рабочего потока может быть оценена по критерию Фруда:
Frкр = ≥ 10-5,
(18.10.17)
В табл. 18.10.4. приведена оценка пределов скорости потока для различных геометрических размеров элементарной ячейки при рабочей температуре 10°С и Rекр = 3000 > 2800.
Таблица 18.10.4.
| H, см |
В, см |
B / H |
Rг, см |
Vmin, см/с |
Frкр1 |
| 1 |
1 |
1 |
0,250 |
39,240 |
6,278 |
| 2 |
2 |
0,333 |
29,430 |
2,649 |
| 5 |
5 |
0,417 |
23,544 |
1,356 |
| 10 |
10 |
0,455 |
21,582 |
1,045 |
| 20 |
20 |
0,476 |
20,601 |
0,909 |
| 50 |
50 |
0,490 |
20,012 |
0,833 |
177
Продолжение табл. 18.10.4
| H, см |
В, см |
B / H |
Rг, см |
Vmin, см/с |
Frкр1 |
| 1,5 |
1,5 |
1 |
0,375 |
26,160 |
1,860 |
| 3 |
2 |
0,500 |
19,620 |
0,785 |
| 7,5 |
5 |
0,625 |
15,696 |
0,402 |
| 15 |
10 |
0,682 |
14,388 |
0,310 |
| 30 |
20 |
0,714 |
13,734 |
0,269 |
| 75 |
50 |
0,735 |
13,342 |
0,247 |
| 2 |
2 |
1 |
0,500 |
19,620 |
0,785 |
| 4 |
2 |
0,667 |
14,715 |
0,331 |
| 10 |
5 |
0,833 |
11,772 |
0,170 |
| 20 |
10 |
0,909 |
10,791 |
0,131 |
| 40 |
20 |
0,952 |
10,301 |
0,114 |
| 100 |
50 |
0,980 |
10,006 |
0,104 |
| 2,5 |
2,5 |
1 |
0,625 |
15,696 |
0,402 |
| 5 |
2 |
0,833 |
11,772 |
0,170 |
| 12,5 |
5 |
1,042 |
9,418 |
0,087 |
| 25 |
10 |
1,136 |
8,633 |
0,067 |
| 50 |
20 |
1,190 |
8,240 |
0,058 |
| 125 |
50 |
1,225 |
8,005 |
0,053 |
При выполнении расчетов, аналогичных приведенным в табл. 18.10.4, значение Re принимается большим, нежели Reкр, поскольку в процессе работы геометрические размеры элементарной ячейки меняются в сторону увеличения высоты (Н) за счет растворения материала электродов. Пределы этих изменений можно оценить по принимаемой толщине электродных пластин (δ).
Например, примем толщину рабочего электрода δ = 6 мм = 0,6 см. и зададим параметры элементарной ячейки: В = 1см, H = 1см, что соответствует гидравлическому радиусу элементарной ячейки Rг = 0,25 см. При этом для Reкр = 2800 минимально допустимая скорость потока жидкости будет составлять vmin = 36,624 см/с. То есть в начальный период работы аппарата допустимые критические параметры нарушаться не будут. Однако после того, как электрод сработается, например, на 5 мм, высота элементарной ячейки станет равной H = 1,5 см, а гидравлический радиус Rг = 0,30 см. Рабочая скорость потока при этом уменьшится и будет равна vp = 24,416 см/с. Величина критерия Рейнольдса для потока в этих условиях окажется равной Re = 2240, что на 20% меньше Reкp = 2800. Такое изменение гидродинамических режимов потока недопустимо, поскольку приведет к нестабильности работы установки, т.к. будет сопровождаться повышением поляризуемости рабочих электродов, снижением действительных рабочих плотностей рабочего тока и количества генерируемого коагулянта и т.п.
Помимо названного выше, выбранное значение (Н) проверяется на обеспечение безопасных величин напряжения питания (U ≤ 36 В).
Зная допустимые скорости обрабатываемого потока (vmin) и площадь сечения элементарной ячейки (Sэ = В · H), можно определить расход жидкости через элементарную ячейку (qэ) и рассчитать количество ячеек (nэ.я), необходимое для обеспечения заданной производительности установки.
qэ = Sэ · vmin = (B · H) · vmin,
(18.10.18)
nэ.я = Q / qэ,
(18.10.19)
Если расчетная пэ.я не является целым числом, то проводят его округление до целочисленного значения с проверкой vmin на удовлетворение критическим параметрам
178
работы. При необходимости могут изменяться выбранные параметры элементарной ячейки с пересчетом всех критических характеристик.
Длина рабочих электродов (lэ) определяется исходя из рассчитанной величины рабочей поверхности (Sа).
Поскольку известна (выбрана) ширина элементарной ячейки (В) и рассчитано необходимое количество ячеек (nэ.я), рабочая ширина всех электродов в аппарате (Bраб) равна:
Bраб = В · nэ.я,
(18.10.20)
Так как
Sа = Bраб · lэ,
(18.10.21)
то
lэ = Sa / Bраб.
(18.10.22)
Если расчетная величина (lэ) оказывается слишком большой из конструктивных или строительных соображений, то возможно разбиение ее на блоки, суммарная длина которых равна (lэ).
После определения установочных (задаваемых) и основных технологических параметров аппарата, приведенных выше можно производить расчет его конструктивных и строительных параметров.
Для этого необходимо принять общую конструкторскую схему аппарата и выбрать принципиальную схему соединения электродов. Чаще всего на практике для генераторов коагулянта используют проточные аппараты с продольным, восходящим или нисходящим направлением движения жидкости и набором плоскопараллельных электродов в рабочей зоне аппарата. Принципиальная схема аппарата представлена на рис. 18.10.9.
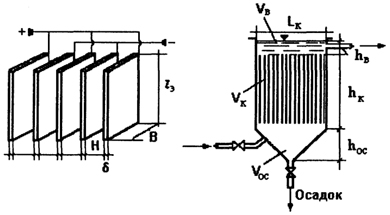
Рис. 18.10.10. Расчетная схема генератора коагулянта.
Количество электродов, которые образуют проходные элементарные ячейки и размещаются в рабочей камере генератора можно определить по выражению:
N = nэ.я + 1,шт.
(18.10.23)
Генератор конструктивно имеет прямоугольную форму. Длина (Lк), ширина (Вк) и высота (hг) аппарата зависят от метода компоновки элементарных ячеек в корпусе генератора.
При однорядной продольной компоновке элементарных ячеек длина аппарата будет определяться выражением:
Lк = [(H + δ) · nэ.я] + 2 м,
(18.10.24)
где м - величина монтажного зазора, обычно равна 5-10 мм.
Ширина аппарата:
Вк = В + 2 м,(18.10.25)
При однорядной поперечной компоновке эти же величины соответственно равны:
Lк = H + 2δ + 2 м,
(18.10.26)
179
Вк = (В · nэ.я) + 2 м,
(18.10.27)
При многорядной смешанной компоновке длина и ширина аппарата будут кратны соответствующим характеристикам элементарной ячейки. Соответствующие соотношения подбираются исходя из других условий, например размеров и конфигурации площади помещения, в котором будет размещен аппарат.
Высота аппарата во всех случаях одинакова и равна:
hг = hос + hк + hв,
(18.10.28)
где hос - высота осадочной зоны, м, (принимается конструктивно при угле наклона конуса 45-60°); hк - высота рабочей камеры, м, (принимается равной (1,05-1,1) · lэ); hв - высота верхней зоны, м, (принимается равной (0,1-0,2) · lэ).
Масса электродов генератора коагулянта (Мэл) рассчитывается по выражению:
Мэл = δ · Sа · ρ,
(18.10.29)
где ρ - плотность материала электродов, т/м3, (ρFe = 7,86, ρAl = 2,58).
Срок службы электродов до замены (τраб) может быть определен по выражению:
τраб = Мл · ηмет / Дк · Qчас,
(18.10.30)
где ηмет - коэффициент полезного использования металла, (ηмет = 0,8-0,9); Дк - доза коагулянта, генерируемого в обрабатываемый поток, г/м3; Qчас - часовая производительность аппарата, м3/ч.
Кроме аналитического метода расчета основных параметров аппаратов электрохимической генерации коагулянта в литературе встречаются и графические методы расчета.
На рис. 18.10.10-18.10.12 приведены рекомендованные в /2/ номограммы для определения основных конструктивных параметров электрореакторов в зависимости от необходимой производительности оборудования и основных электрохимических характеристик рабочих материалов.
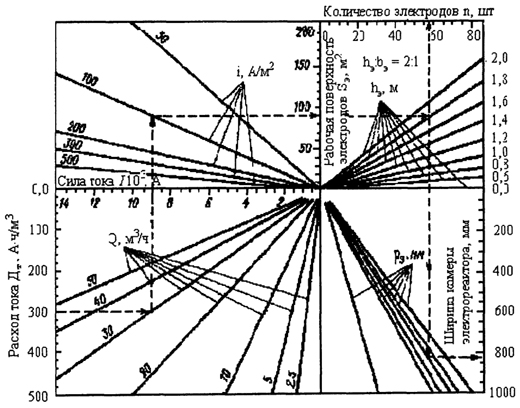
Рис. 18.10.10. Номограмма для определения основных конструктивных параметров электрореакторов в зависимости от расхода воды и электрических параметров их работы.
180
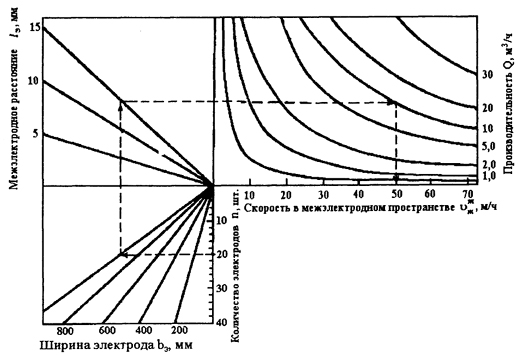
Рис. 18.10.11. Номограмма для расчета скорости движения воды в межэлектродном пространстве электрореактора с плоскопараллельными электродами.
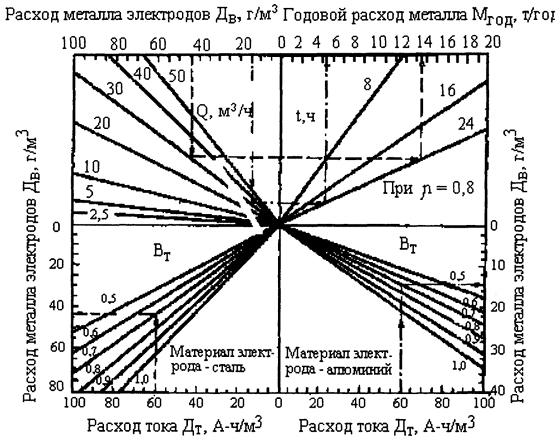
Рис. 18.10.12. Номограмма определения расхода металла электродов.
Использование графического метода расчетов позволяет с достаточно высокой инженерной точностью получить необходимые конструктивные параметры аппаратов.
Подбор необходимых источников тока для питания электрогенераторов коагулянта производится на основании величин рабочих токов и рабочих напряжений, необходимых для обеспечения нормального функционирования аппаратов. В табл. 18.10.5
181
приведены технические параметры некоторых выпрямительных агрегатов, выпускаемых нашей промышленностью.
